



2023年6月,瑞思德在生命科学领域的期刊《生命的化学》上发表了题为“免疫衰老及免疫细胞在衰老中的作用”的研究论文。
研究团队综述了免疫衰老以及免疫细胞在衰老中作用的研究进展,旨在阐明免疫衰老与衰老相关疾病的关系及免疫细胞的抗衰老机制,为精准免疫细胞抗衰老模式提供临床应用的新策略。
什么是免疫衰老?
在衰老过程中,免疫细胞容易受到内源性DNA损伤,会逐渐失去清除病原体和癌细胞的能力,这种现象就是免疫衰老。
免疫衰老特征:
² 抗原呈递障碍
² 幼稚T细胞(naïve T cells)启动
² CD8+ T细胞细胞毒性功能减弱
² 幼稚B细胞和T细胞的收缩
² 高酸度抗体的产生量减少
不同免疫细胞在衰老中的作用
淋巴细胞是免疫系统的基本成分,在体内分布很广泛,主要是T淋巴细胞、
B淋巴细胞受抗原刺激而被活化,分裂增殖、发生特异性免疫应答。除T淋巴细胞和B淋巴细胞外,还有K淋巴细胞和NK淋巴细胞,共四种类型。
T细胞在衰老中的作用
人体血液中,T细胞约占免疫细胞的7%-24%,占淋巴细胞的70%,是淋巴细胞的主要组分。它具有多种生物学功能,如直接杀伤靶细胞、辅助或抑制B细胞产生抗体、对特异性抗原和促有丝分裂原的应答反应以及产生细胞因子等,是身体中为抵御疾病感染、肿瘤而形成的“英勇斗士”。
T细胞产生的免疫应答是细胞免疫,细胞免疫的效应形式主要有两种:一种是与靶细胞特异性结合,破坏靶细胞膜,直接杀伤靶细胞;另一种是释放淋巴因子,最终使免疫效应扩大和增强。
不过随着年龄的增长,体内的T细胞会逐渐老化。
Ø T细胞衰老的特征
² 幼稚T淋巴细胞减少
² 晚期高分化记忆T淋巴细胞增多
² 线粒体DNA损伤
² 胸腺退化
² 效应/记忆T细胞的积累
² T细胞受体(T cell receptor,TCR)功能下降
² 端粒酶活性降低
² 端粒缩短
² DNA损伤
衰老T细胞表达的标志物是CD57和KLRG-1等,这些标志物的上调表明复制性衰老,即细胞多次分裂之后增殖能力下降,最终分裂完全停止。
B细胞在衰老中的作用
在骨髓中,多能造血干细胞 (multiplehematopoietic stem cells,HSCs)分化为B淋巴细胞祖细胞,进一步分化为祖B细胞(pro-B细胞)、前体B细胞(pre-B细胞)和未成熟B细胞。
B细胞亚群包括B-1、B-2和调节性B细胞。
² B-1细胞主要来源于胎儿肝脏,包含B-1a和B-1b亚群。
² B-2细胞来源于骨髓(BM),可进一步分为滤泡B(follicular B,FOB)和边缘B区(marginalzoneB,MZB)细胞。
² 调节性B细胞的功能是抑制免疫反应(通过产生抗炎细胞因子IL-10)。
B细胞衰老的一个主要标志是骨髓内B淋巴细胞生成的丧失。在衰老过程中,由于重组激活基因(RAG)和替代轻链(SLC)表达的下调或完全丧失,前B细胞受体(pre-BCR)和B细胞受体(BCR)发育受到影响,而这两种基因决定了B细胞的成熟(图1B)。
NK细胞在衰老中的作用
NK细胞可以根据表面标记物CD56和CD16的表达进行细分,其中CD56dim NK细胞具有细胞毒性,而CD56bright NK细胞主要负责细胞因子(如IFN-γ和TNF-α)的分泌。
随着年龄的增长,NK细胞分泌IFN-γ、TNF、IL-2和IL-12,表达IL-2R的能力均有所下降。
² IFN-γ:活化巨噬细胞、抗病毒、促进MHC分子表达和抗原呈递、诱导Th1细胞分化和抑制Th2细胞分化等。
² TNF:参与调节适应性免疫应答、杀伤靶细胞和诱导细胞凋亡过程。
² IL-2:含量下降会造成自身反应性T细胞增殖,诱发自身免疫性疾病(图1C)。
NK细胞本身寿命较短(约两周),免疫衰老的NK细胞表现出细胞因子分泌减少和靶细胞毒性降低的功能障碍特征。NK细胞是衰老细胞免疫监视的主要参与者,随着年龄的增长而增加,并且伴随端粒缩短和端粒酶活性降低。
早期的研究依赖CD16来区分NK细胞和其他淋巴细胞,这可能导致了NK细胞总数检测不完整。然而,随着技术的发展,比起CD16,人们认为CD56是更可靠和通用的人类NK细胞标志物。虽然CD16通常在更成熟的亚群CD56dim室中表达,但CD56bright NK细胞亚群有时缺乏或低表达CD16。
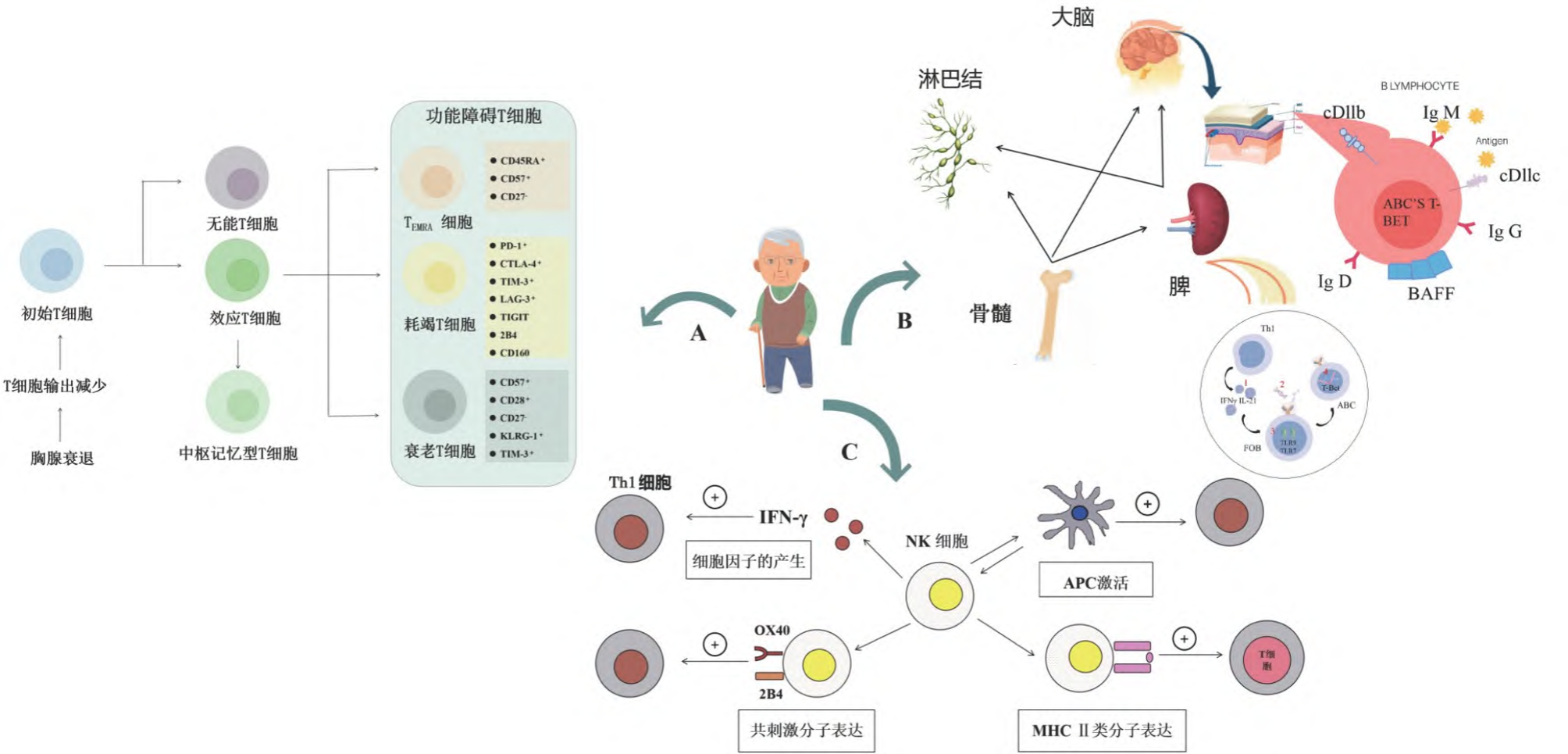
图1 不同免疫细胞在衰老中的作用
免疫衰老与衰老相关疾病
免疫衰老与神经退行性疾病
免疫衰老(特别是炎症性衰老)与神经退行性疾病和认知能力下降有关。前人针对873名70-90岁无痴呆患者的人群展开调查分析,白细胞介素(IL-6、IL-10、IL-12、IL-1β)和肿瘤坏死因子-α(TNF-α)的高表达人群往往认知功能低。其潜在机制可能是长期和/或过量的促炎因子释放到中枢神经系统,导致脑源性神经营养因子的表达降低,该因子与神经发生、谷氨酸激活、氧化应激和凋亡诱导有关。
先前的一项研究通过计数阿尔茨海默病患者的外周血单个核细胞(PBMC)的数量来描述免疫特征:CD8+ T效应记忆CD45 RA+细胞的增加。这些细胞聚集在大脑的Aβ斑块附近,并与认知能力呈负相关。
免疫衰老与心脑血管疾病
动脉粥样硬化是一种典型的炎症性疾病,是心血管疾病的病理基础,在老年人中极为常见。这种炎症性疾病可能是由某些自身抗原(如Hsp65修饰的低密度脂蛋白)或感染因子(如肺炎衣原体)引起的。
以往相关研究表明:
1) 免疫衰老过程中具有SASP的衰老T细胞会导致动脉粥样硬化的发生。
2) 随着疾病的发生,单核细胞/巨噬细胞具有持续的促炎症行为,外周血单核细胞的炎症性质可以预警心血管疾病的发生。
3) 在慢性心力衰竭(CHF)病程中,单核细胞表达TLR-4增加,可能与血浆中IL-1、IL-6和TNF等促炎细胞因子的水平增加有关,可以预测CHF患者的长期生存率,而随着年龄的增长,白细胞的TLR系统也发生了类似的变化。
免疫衰老与代谢性疾病
免疫衰老与代谢紊乱之间具有明显的相关性。内分泌衰老调节免疫系统,免疫衰老改变内分泌系统,形成一个恶性循环。
以往相关研究表明:
1) 过多的雄激素产生和胰岛素抵抗参与了衰老相关的代谢性疾病的发生。
2) 2型糖尿病(T2DM)实际上就是免疫衰老相关疾病。其典型特征是CD4+幼稚T细胞库的减少,并伴随着效应CD4+/CD8+ T细胞和记忆CD4+ T细胞库的增加。
3) 衰老或晚期分化的T细胞(CD8+CD28–、CD8+CD57+)可以用于预测人类的高血糖。
4) 肥胖人群中糖化血红蛋白表达的增加与中性粒细胞和单核细胞的吞噬功能的降低有关,而二甲双胍治疗能逆转糖化血红蛋白的表达。
5) 肥胖个体的血浆介质可能促进免疫衰老的早期发生。肥胖人群血浆中健康外周血单个核细胞CD28表达减少,晚期分化的CD8+CD28–T细胞数量增加。
免疫衰老与肿瘤
免疫监视:免疫细胞可以检测和控制缺陷或衰老的细胞,从而避免肿瘤细胞的发展。免疫系统可以负责识别和消除癌症前体,主要由细胞毒性NK细胞和CD8+ T细胞调控。
免疫编辑:另一方面,在癌细胞的形成和发展过程中,免疫细胞和癌细胞之间会发生相互作用。肿瘤免疫编辑包括消除、平衡和肿瘤逃逸,这些过程均受免疫衰老的影响。
因此,免疫监测不良是免疫衰老不可忽视的组成部分,这是癌症发生的机制之一。
小结及展望
衰老导致的必然结果是与年龄相关的慢性疾病的发生(心血管疾病、癌症、神经退行性疾病和糖尿病等)。衰老与免疫细胞变化密切相关,其特征是先天性和适应性免疫细胞的表型和功能发生多种变化。随着年龄的增长,免疫系统发生细胞亚群和功能的改变,其功能逐渐衰退,并表达相应的免疫衰老相关指标。
本文建议:1、通过补充免疫细胞来清除衰老细胞,提高机体的免疫应答能力;2、通过检测外周血淋巴细胞亚群指标的变化,有助于筛选亚临床状态的人群和对重大疾病的预防,指导临床疗效的判定。
希望进一步了解人类免疫细胞衰老机制以及免疫治疗在临床上的应用,并找到改善衰老及衰老性相关疾病治疗的关键途径。